|
Con el agotamiento de la reserva funcional aparece la disfunción del ventrículo izquierdo que provoca la disminución del gasto cardíaco y de la presión arterial sistémica. Como consecuencia, se activan diferentes sistemas neurohormonales compensadores para tratar de aumentar la presión arterial y la perfusión tisular: el sistema barorreceptor sistema nervioso simpático, el sistema renina angiotensina aldosterona y el sistema arginina vasopresina
Estos sistemas incrementan la frecuencia cardiaca, la contractilidad miocárdica, producen vasoconstricción y retención de sal y agua. Al principio, estos mecanismos compensadores mantienen el gasto cardiaco y la presión arterial, pero, a la larga incrementan el trabajo cardíaco y la pérdida de miocitos, lo que origina un círculo vicioso que perpetúa los mecanismos y provoca la progresión de la enfermedad.
El tratamiento farmacológico actual se basa en el bloqueo de estos sistemas neurohormonales con el objetivo de interrumpir el progreso y mejorar el pronóstico. Este es el caso de los IECA, los bloqueadores de los receptores de angiotensina II (ARA-II) y los antagonistas de la aldosterona (espironolactona y epleronona) que actúan en el sistema renina-angiotensina-aldosterona y los bloqueadores betaadrenérgicos que actúan bloqueando la respuesta simpática. De hecho, estos agentes han demostrado en los ensayos clínicos ser beneficiosos para mejorar el pronóstico.
Los péptidos natriuréticos:
Las hormonas natriuréticas (A, B y C) son una familia de péptidos vasoactivos que se sintetizan en el corazón ante situaciones de sobrecarga que provoca una distensión de los miocitos auriculares. Estas sustancias actúan a nivel del riñón induciendo natriuresis para disminuir el volumen circulante y por efecto feedback disminuir la distensión auricular (35).
Actualmente estas sustancias están siendo intensamente investigadas en tres sentidos: como factor pronóstico, como marcadores para el diagnóstico y como tratamiento.
Una revisión sistemática recientemente publicada (36) señala que el péptido natriurético tipo B (BNP) es un fuerte indicador pronóstico para pacientes con IC en cualquier estadío de la enfermedad y un mejor predictor de supervivencia que muchos indicadores pronósticos tradicionales como la clase funcional de la NYHA, la creatinina sérica y la FE del VI. El riesgo relativo de muerte se incrementa en un 35 % por cada 100 pg/ml de elevación del BNP en estos pacientes.
La medición de las concentraciones plasmáticas de péptidos natriuréticos (el BNP y el fragmento N terminal del pro-BNP) puede ayudar al diagnóstico de IC, especialmente en salas de urgencias: un paciente con disnea y concentraciones normales de péptidos natriuréticos descarta la IC (37).
Como medicamento, el nesiritide (BNP humano recombinante) ha demostrado ser útil en el tratamiento de la IC aguda por sus efectos vasodilatadores y utilizado en bolos a dosis de 2 mg/kg seguido de infusión de 0,015-0,03 mg/kg/min. El efecto adverso más temible es la hipotensión prolongada (38).
La clínica :
La presentación clínica de la IC varía de acuerdo al terreno donde asienta. En pacientes con buen validismo funcional suele presentarse con los síntomas y signos típicos: disnea de esfuerzo, ortopnea, disnea paroxística nocturna, reducción de la tolerancia al ejercicio, letargia, fatiga, tos nocturna, hinchazón de las piernas, anorexia, taquicardia, pulso alternante, distensión venosa yugular, latido de la punta desplazado, crepitantes y/o sibilancias, tercer o cuarto ruido cardiaco, edema periférico, hepatomegalia sensible o ascitis.
No obstante, cada día es más frecuente que se presente en ancianos con polimorbilidad, deterioro funcional o cognitivo y polifarmacia por lo que la obtención de los datos de la historia clínica resulta más laboriosa y los síntomas y signos de presentación pueden ser atípicos.
Entre las peculiaridades de la historia clínica en el anciano es un hecho que tenemos que dedicarle más tiempo y contar con el acompañante para completar y precisar los datos, hay que tener en cuenta la posible ausencia de síntomas habituales, la mayor frecuencia de manifestaciones inespecíficas y de manifestaciones anterógradas (39).
La atipicidad puede manifestarse de diferentes maneras: en el anciano inmóvil puede faltar la disnea, la confusión mental puede ser una forma de presentación frecuente en los ancianos que tienen de base algún grado de deterioro cognitivo, el deterioro brusco de las actividades de la vida diaria, la asociación frecuente con neumonía que es un factor confundente para el diagnóstico y la presentación como acompañante de otros síndromes geriátricos como las caídas, la inmovilización y la incontinencia.
En el anciano con IC, la valoración geriátrica integral constituye una herramienta valiosa al determinar la situación física, mental y social del paciente que tanto tienen que ver con su calidad de vida y con sus capacidades para enfrentar la enfermedad, además de precisar las enfermedades asociadas, el estado nutricional y el tratamiento farmacológico previo, que están muy relacionados con las decisiones terapéuticas futuras y la respuesta al tratamiento.
Desde el punto de vista práctico, resulta útil la orientación que brinda al médico el árbol de decisiones que se muestra a continuación.
Avances en el tratamiento:
El tratamiento de la IC ha cambiado considerablemente en la última década como resultado de numerosos ensayos clínicos que han añadido medicamentos útiles al arsenal terapéutico y por un cambio de objetivos que además de mejorar la sintomatología, intenta evitar la progresión de la enfermedad y disminuir su mortalidad (40).
Los diuréticos son imprescindibles para el alivio de los síntomas congestivos prácticamente en todos los pacientes con IC sintomática.
Los diuréticos bloqueadores de los receptores de aldosterona, han mostrado reducir la mortalidad por IC grave (Clase III-IV de la NYHA). El estudio RALES de 1999 demostró un 30 % de reducción de la mortalidad con el uso de dosis bajas de espironolactona (25-50 mg diarios) en pacientes con IC que ya estaban tomando un IECA (41). Más recientemente el ensayo EPHESUS (42) utilizó la eplerenona, un bloqueador de los receptores de aldosterona que no produce ginecomastia en pacientes con infarto del miocardio y disfunción del VI con resultados positivos en términos de disminución de la mortalidad.
Los IECA tienen muchos beneficios, al reducir la producción de Angiotensina-II y posiblemente al incrementar la producción de bradikinina, actuando tanto en el remodelado como en la inhibición del sistema renina-angiotensina-aldosterona.
Los ensayos CONSENSUS (43), SOLVD (44), V-HeFT II (45) y SAVE (46) han demostrado que estos agentes mejoran los síntomas y reducen la hospitalización y la mortalidad entre un 16 y un 28 %. Actualmente se recomiendan para todos los pacientes con disfunción sistólica salvo complicaciones como disfunción renal severa, hipotensión sintomática, hiperpotasemia, tos intolerante y edema angioneurótico.
 Los ARA II bloquean el efecto de la Angiotensina-II a nivel del receptor específico AT1. Contrario a lo que cabría esperarse, el estudio ELITE II (47) no pudo demostrar superioridad de estos agentes con respecto a los IECA en la IC. Recientemente los ensayos Val FET (48) y CHARM (49) encontraron que la combinación de un ARA-II con un IECA tiene el beneficio adicional de disminuir la tasa de hospitalizaciones con respecto a las obtenidas con IECA solos. Como quiera que los ARA-II son más caros que los IECA, actualmente se recomienda su uso como tratamiento alternativo en pacientes en que estén contraindicados los IECA o exista intolerancia a estos.
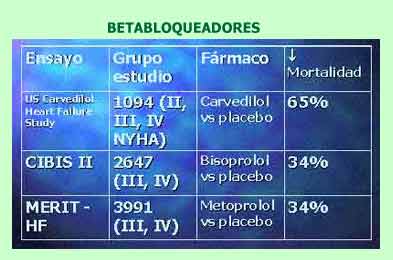 Los betabloqueadores, por mucho tiempo contraindicados en la IC por sus efectos inotrópicos negativos, hoy forman parte indiscutible del arsenal terapéutico de este síndrome. Los ensayos clínicos US Carvedilol Heart Failure Study (50), CIBIS-2 (51), MERIT-HF (52) y COPERNICUS (53) han utilizado los agentes bisoprolol, metoprolol y carvedilol y han aportado evidencias definitivas que confirman la aparición de importantes efectos beneficiosos sobre la calidad de vida, la morbilidad y la supervivencia de los pacientes.
La combinación de un IECA y un betabloqueador es en la actualidad la piedra angular del tratamiento de los pacientes con IC por disfunción sistólica del VI (15).
Todo paciente con disfunción sistólica del VI y síntomas leves o moderados (Clase II-III de la NYHA) con tratamiento convencional (diuréticos + IECA) debe ser tratado con betabloqueadores siempre y cuando el paciente se haya mantenido en un período de estabilidad clínica aproximadamente un mes y no existan contraindicaciones como asma, EPOC o bloqueo aurículoventricular (40). Deben usarse dosis bajas de inicio que se aumentarán progresivamente cada dos semanas.
En fecha más reciente se realizó el ensayo COMET (54) que comparó dos betabloqueadores: carvedilol vs metoprolol. El carvedilol se mostró superior al metoprolol en reducir la mortalidad tras un seguimiento de 5 años.
La digoxina, un medicamento utilizado durante décadas por sus propiedades inotropas positivas, en el momento actual ha pasado a ser de segunda línea, después de la publicación en 1997 de los resultados del ensayo DIG (55). Esta investigación estudió cerca de 6000 pacientes con IC por disfunción sistólica que estaban recibiendo un IECA y un diurético, los que se asignaron aleatoriamente a digoxina o placebo. Este estudio encontró, después de un seguimiento de 37 meses que no existieron diferencias en la mortalidad en ambos grupos, sin embargo, en el grupo tratado con digoxina hubo menos hospitalizaciones (56).
Las guías actuales (16) recomiendan el uso de digoxina para aquellos pacientes que permanecen sintomáticos aún usando diuréticos, IECA y betabloqueadores (Nivel de evidencia: B). Se plantea que la digoxina tiene un papel limitado en los pacientes con ritmo sinusal (15) y que su indicación más precisa es en aquellos que tienen fibrilación auricular con respuesta ventricular rápida.
Los vasodilatadores del tipo de los nitratos y la hidralazina son menos efectivos que los IECA para mejorar la supervivencia (57) y actualmente se recomiendan como alternativos para aquellos pacientes con síntomas de IC por disfunción sistólica del VI que son intolerantes a los IECA y a los ARA-II (Nivel de evidencia: C) (16).
Los estudios con antagonistas de la endotelina (tezosentán, bosentán) (58) y con antagonistas del TNF-a (etanercept, infliximab) (59) han sido un fracaso. Los primeros producen hepatotoxicidad y no disminuyen la mortalidad, mientras que los segundos están actualmente contraindicados pues incrementan el riesgo de muerte y de hospitalización.
El levosimedan, un nuevo agente inotrópico con acción inhibidora de la fosfodiesterasa y sensibilizador del calcio se ha utilizado en bolos e infusión intravenosa continua en pacientes con IC avanzada y refractaria, con mejoría de la supervivencia a los 180 días (38, 40).
Los anticálcicos de primera generación (nifedipina, verapamilo y diltiazem) no se recomiendan en los pacientes con IC por disfunción sistólica por sus efectos inotropos negativos y la inducción de taquicardia refleja, lo que agrava el cuadro clínico (40).
Otros tratamientos:
Algunas revisiones sistemáticas han encontrado que el entrenamiento de ejercicios disminuye la mortalidad y mejora el desempeño de los pacientes con IC (60). Los individuos estudiados son pocos, altamente seleccionados y con buenos recursos en centros académicos, por lo que es difícil extrapolar estos resultados a la población comunitaria.
Los programas multidisciplinarios reducen todas las causas de mortalidad y las hospitalizaciones, lo mismo por IC que por cualquier causa (60).
El trasplante cardiaco (TC) es una opción terapéutica que mejora considerablemente el pronóstico en aquellos pacientes con IC refractaria que cumplen determinados criterios de selección como que no existan patologías asociadas que contraindiquen el TC, que no se haya realizado previamente ninguna cirugía reparadora, que la FE > 20 % y la VO2 max > 14 ml/kg/min y que en las pruebas de cateterismo cardiaco no exista una hipertensión pulmonar irreversible (40). Los trasplantados tienen una supervivencia al año de un 80 % y de 66 % a los 10 años (32). Sin embargo, la escasez de donantes y, obviamente, la mayoría de casos (ancianos polimórbidos) que no cumplen los criterios de inclusión, hacen que esta no sea una solución para la masa crítica de pacientes con esta afección.
Cerca de la mitad de los pacientes con IC tienen una muerte súbita causada por trastornos del ritmo. Para estos pacientes existen dos opciones: la colocación de un desfibrilador automático implantable (DAI) o el uso de amiodarona en aquellos que no sean candidatos a los DAI que, por lo demás, son altamente costosos.
Los trastornos de la conducción intraventricular, en particular la presencia de bloqueo de rama izquierda, son frecuentes en pacientes con IC. Está planteado que estos trastornos provocan una asincronía en la contracción ventricular que provoca disminución del rendimiento. La llamada resincronización cardiaca se consigue estimulando simultáneamente ambos ventrículos mediante electrodos introducidos a través del seno coronario. Este tratamiento mejora la FE y el gasto cardiaco, reduce las hospitalizaciones, pero no disminuye la mortalidad (61).
Por último, un tratamiento que parece tener perspectivas futuras es el trasplante celular de mioblastos antólogos o células madre de la médula ósea en zonas infartadas coincidiendo con una cirugía de revascularización coronaria. Todavía no existen evidencias de que este tratamiento pueda ser efectivo debido al escaso número de casos en los que se ha practicado.
Conclusiones:
A pesar de los avances en el conocimiento de la fisiopatología y en la adquisición de nuevas modalidades teapéuticas, la IC continúa siendo un gran síndrome y un gran reto para la medicina de nuestros tiempos.
El reconocimiento de que este síndrome será cada día más frecuente y constituirá una forma habitual de morir, en una población mundial que a ojos vista envejece, debe poner en alerta la conciencia de la profesión médica a no cejar en las investigaciones en este campo.
Bibliografía:
- Davies RC, Hobbs FDR, Lip GYH. ABC of heart failure. History and epidemiology. BMJ 2000; 320: 39-42.
- Aldama López G, Piñeiro Portela M, Campo Pérez Esteban P. Insuficiencia cardiaca: concepto, epidemiología, clasificación, etiología y fisiopatología. Medicine 2005; 9(35): 2279-90.
- Romero Cabrera AJ. Insuficiencia cardiaca en el anciano. Geriatrianet.com. Revista Electrónica de Geriatría 2002; 4(1): 1-30. URL disponible en http://www.geriatrianet.com/numero6/privado6/geriatriaarticulo%202002_1.html.
- Ho KK, Pinsky JL, Kannel WB, Levy D. The epidemiology of heart failure: the Framingham Study. J Am Coll Cardiol 1993; 22: 6A-13.
- Abdelhafis AH. Heart failure in older people: causes, diagnosis and treatment. Age Aging 2000; 31: 29-36.
- Rodríguez Artalejo F, Banegas Banegas JR, Guallar Castillón P. Epidemiología de la insuficiencia cardiaca. Rev Esp Cardiol 2004; 57: 163-170.
- Manzano L, Sánchez Mateo D, Rodríguez González P. La insuficiencia cardiaca en la práctica asistencial del internista. Rev Clin Esp 2005; 205 (7): 305-6.
- Jessup M, Brozena S. Heart failure. N Engl J Med 2003; 348 (20): 2007-2018.
- Basile JN. Heart failure: a three-article symposium. Postgrad Med 200·; 113(3): 50.
- Cowie MR, Fox KF, Wood DA, et al. Hospitalizations of patients with heart failure: a population-based study. Eur Heart J 2002; 23: 877-85.
- Lee DS, Mamdani MM, Austin PC, et al. Trends in heart failure outcomes and pharmacotherapy : 1992 to 2000. Am J Med 2004; 116: 581-89.
- Bleumink GS, Knetsch AM, Sturkenboom MC, et al. Quantifying the heart failure epidemic: prevalence, incidence rate, lifetime risk and prognosis of heart failure. Eur Heart J 2004; 25: 1614-19.
- Roger VL, Weston SA, Redfield MM, et al. Trends in heart failure incidence and survival in a community-based population. JAMA; 292: 344-50.
- Osca Asensi J, Cuéllar de León AJ. Factores pronósticos en la insuficiencia cardiaca. SEMERGEN 2004; 30(9): 437-43.
- McMurray JJV, Pfeffer MA. Herat failure. Lancet 2005; 365: 1877-89.
- Hunt SA, Abraham WT, Chin MH, Feldman AM, Francis GS, Ganiats TG, et al. ACA/AHA 2005 Guideline update for the diagnosis and management of chronic heart failure in the adult Summary Article. J Am Coll Cardiol 2005; 46: 1116-1143.
- Negrín JE, Cordiés L, Roselló N, Sánchez J, Negrín JA. Insuficiencia cardiaca crónica. Rev Cubana Med 2001; 40(3): 195-211.
- Hogg K, Swedberg K, McMurray J. Heart failure with preserved left ventricular systolic function; epidemiology, clinical characteristics, and prognosis. J Am Coll Cardiol 2004; 43: 317-27.
- Kitzman DW, Little WC, Burbaker PH, Anderson RT, Hundley WG, Marburger CT, et al. Pathophysiological characterization of isolated diastolic heart failure in comparison to systolic heart failure. JAMA 2002; 288: 2144-2150.
- Cleland JG, Swedberg K, Follath F, Komajda M, Cohen-Solal A, Aguilar JC, et al. The euroheart failure survey program a survey on the quqlity of care among patients with heart failure in Europe. Part 1: patients characteristics and diagnosis. Eur Heart J 2003; 24: 442-463.
- McMurray JJV, Pfeffer MA. The year in heart failure. J Am Coll Cardiol 2004; 44: 2398-2405.
- Zile MR. Heart failure with preserved ejection fraction: is this diastolic failure?. J Am Coll Cardiol 2003; 41: 1519-1522.
- Zile MR, Baicu CF, Gaasch WH. Diastolic heart failure abnormalities in active relaxation and passive stiffness of the left ventricle. N Engl J Med 2004; 350: 1953-9.
- Kass DA, Bronzwaer JGF, Paulus WJ. What mechanisms underlie diastolic dysfunction in heart failure. Circulation Res 2004; 94: 1533-43.
- Redfield MM, Jacobsen SJ, Burnett Jr JC, Mahoney DW, Bailey KR, Rodeheffer RJ. Burden of systolic and diastolic ventricular dysfunction in the community: appreciating the scope of the heart failure epidemic. JAMA 2003; 289: 194-202.
- Lenzen MJ, Scholte op Reimer WJ, et al. Differences between patients with a preserved and a depressed left ventricular function: a report from the EuroHeart Failure Survey. Eur Heart J 2004; 25: 1214-20.
- Masoudi FA, Hawanek EP, Smith G, Fish RH, Steiner JF, Ordin L, et al. Gender, age and heart failure with preserved ventricular systolic function. J Am Coll Cardiol 2003; 41: 217-223.
- European Study Group on Diastolic Heart Failure. How to diagnose diastolic heart failure. Eur Heart J 1998; 19: 990-1003.
- Pantilat SZ, Steimle AE. Palliative care for patients with heart failure. JAMA 2004; 291: 2476-82.
- Gibelin P. An evaluation of symptom classification systems used for the assessment of patients with heart failure in France. Eur J Heart Fail 2001; 3: 739-746.
- Opie LH, Commerford PJ, Gersh BJ, Pfeffer MA. Controversies in ventricular remodelling. Lancet 2006; 367: 356-67.
- Pérez Villa F. Avances en el tratamiento de la insuficiencia cardiaca Med Clin (Barc) 2004; 123(4): 149-53.
- Kaluski E, Kobrin I, Zimlichman R, Marmor A, Krakov O, Milo O, et al. RITZ-5: randomized intravenous TeZosentan (an endothelin.A/B antagonist) for the treatment of pulmonary edema: a prospective, multicenter, doubleblind, placebo-controlled study. J Am Coll Cardiol 2003;41:204-10.
- Mann D. Inflammatory mediators and the failing heart. Past, present, and the foreseeable future. Circ Res 2002;91:988-98.
- Goetze JP, Kastrup J, Rehfeld JF. The paradox of increased natriuretic hormones in congestive heart failure patients: Does the endocrine heart also fail in heart failure?. Eur Heart J 2003; 24: 14711472.
- Doust JA, Pietrzak E, Dobson A, Glasziou P. How well does B type natriuretic peptide predict death and cardiac events in patients with heart failure: systematic review. BMJ 2005; 330: 625-633.
- De Lemos JA, McGuire DK, Drazner MH. B type natriuretic in cardiovascular disease. The Lancet 2003; 362: 316-322.
- Muñoz Rivas N. Manejo del paciente con insuficiencia cardiaca aguda e insuficiencia cardiaca refractaria al tratamiento convencional. JANO 2005; 21 (1580): 49-55.
- Ribera Casado JM. Protocolo de evaluación y tratamiento de la insuficiencia cardiaca en el paciente anciano. Medicine 2003; 8(109): 5857-5859.
- Garrido Bravo JP, Rodríguez Fernández JA, García de Lara J, Castro Beiras A. Tratamiento de la insuficiencia cardiaca crónica. Medicine 2005; 9(35): 2318-2326.
- Pit B, Zannad F, Remme WJ, Cody R, Curbeino A, Pérez A, et al. The effect of spironolactone on morbidity and mortality in patients with severe heart failure. N Engl J Med 1999; 341: 709-17.
- Pit B, Remme W, Zannad F, et al. Eplerenone, a selective aldosterone blocker in patients with left ventricular dysfunction after myocardial infarction. N Engl J Med 2003; 348: 1309-21.
- The CONSENSUS Trial Study Group. Effects of enalapril on mortality in severe congestive heart failure: results of the Cooperative North Scandinavian Enalapril Survival Study (CONSENSUS). N Engl J Med 1987; 316(23): 1429-35.
- The SOLVD Investigators. Effect of enalapril on survival in patients with reduced left ventricular ejection fractions and congestive heart failure. N Engl J Med 1991; 325 (5): 293-302.
- Cohn JN, Jonson G, Ziesche S, et al. A comparison of enalapril with hydralazine-isosorbide dinitrate in the treatment of chronic congestive heart failure. N Engl J Med 1991; 325(5): 303-10.
- Pfeiffer MA, Braunwald E, Moye LA, et al. Effect of captopril on mortality and morbidity in patients with left ventricular dysfunction after myocardial infarction: results of the Survival and Ventricular Enlargement Triald. The SAVE Investigators. N Engl J Med 1992; 327(10): 669-77.
- Pitt B, Poole-Wilson P, Segal R. Effects of losartan vs captopril on mortality in patients with symtomatic heart failure: rationale, design, and baseline characteristics of patients in the Losartan Heart Failure Survival Study ELITE II. J Card Fail 1999; 5(2): 146-54.
- Krum H, Carson P, Fassang C, et al. Effect of valsartán added to background ACE inhibitor therapy in patients with heart failure: result from Val HeFT. Eur J Heart Fail 2004; 6: 937-45.
- Mc Murray JJ, Ostergreen J, Swedberg K, et al. Effects of candesartan in patients with chronic heart failure and reduced left-ventricular systolic function taking angiotensin-converting enzyme inhibitors: the CHARM-Added trial. Lancet 2003; 362: 767-71.
- Packer M, Bristow MR, Cohn JN, et al. The effect of carvedilol on morbidity and mortality in patients with chronic heart failure. N Engl J Med 1996; 334(21): 1349-55.
- The Cardiac Insufficiency Bisoprolol Study II (CIBIS-II): a randomised trial. CIBIS-II Investigators and Committee. Lancet 1999; 353 (9146): 9-13.
- MERIT-HF Study Group. Effect of metoprolol CR/XL in chronic heart failure: Metoprolol CR/XL Randomised Intervention Trial in Congestive Heart Failure (MERIT-HF). Lancet 1999; 353(9169): 2001-7.
- Packer M, Fowler MB, Roecker EB, et al. Effect of carvedilol on the mortality of patients with severe chronic heart failure: results of the Carvedilol Prospective Randomized Cumulative Survival (COPERNICUS) study. Circulation 2002; 106: 2194 99.
- Poole-Wilson P, Swedberg K, Cleland J, Lenarda A, Hanrath P, Komajda M, et al. Comparison of carvedilol and metoprolol on clinical outcomes in patients with chronic heart failure in the Carvedilol Or Metoprolol European Trial (COMET): randomised controlled trial. Lancet 2003;362:7-13.
- Ahmed A. Role of digoxin in older adults with heart failure. Geriatrics and Aging 2002; 5(7): 48 52.
- Garg R, Gorlin R, Smith T, Yusuf S. The effect of digoxin on mortality in patients with heart failure. The Digitalis Investigation Group (DIG). N Engl J Med 1997; 336: 525-33.
- Cohn JN, Jhonson G, Ziesche S, et al. A comparison of enalapril with hydralazine isosorbide dinitrate in the treatment of chronic congestive heart failure. N Engl J Med 1991; 325: 303-10.
- Kaluski E, Kobrin I, Zimlichman R, Marmor A, Krakov O, Milo O, et al. RITZ-5: randomized intravenous TeZosentan (an endothelin.A/B antagonist) for the treatment of pulmonary edema: a prospective, multicenter, doubleblind, placebo-controlled study. J Am Coll Cardiol 2003;41:204-10.
- Mann D. Inflammatory mediators and the failing heart. Past, present, and the foreseeable future. Circ Res 2002;91:988-98.
- Mc Kelvie R. Cardiovascular disorders: Heart failure. Interventions. Clinical Evidence. BMJ Publishing Group Limited 2006. URL disponible en: http://www.clinicalevidence.com. Web publication date: 01/04/2006.
- Bradley D, Bradley E, Baughman K, Berger R, Calkins H, Goodman S, et al. Cardiac resynchronization and death from progressive heart failure. A meta-analysis of randomized controlled trials. JAMA 2003;289:730-40.
|